В Кыргызстане активно внедряется уже несколько лет Электронная база данных лекарственных средств и медицинских изделий (ЭБД), которая стала одной из важнейших реформ в сфере цифровизации фармацевтического сектора. В обиходе все привыкли называть ЭБД «Прослеживаемостью», где модуль Прослеживаемости является только одной частью системы электронного управления фармацевтическим сектором.
Работы над ЭБД были начаты еще в 2018-2019 годах (1 этап) и были основаны на турецкой системе, признанной Всемирной организацией здравоохранения образцовой.
В 2022 году, благодаря поддержке Президента страны, началось активное внедрение 2 этапа ЭБД: в течение шести месяцев была запущена пилотная версия Модуля прослеживаемости, позволяющая отслеживать весь путь лекарства от производства до выдачи пациенту, а в марте 2023 года прослеживаемость уже работала в боевом режиме.
Каждая упаковка имеет уникальный QR-код, по которому можно узнать название препарата, производителя, дату выпуска и серию, импортера и место продажи, а также регулируемую цену, в случае, когда цена лекарства регулируется государством.
Благодаря такой маркировке система фиксирует движение лекарства: пересечение границы, поступление на склад, отправку в аптеку или больницу и выдачу пациенту. После выдачи QR-код деактивируется. Информация хранится в базе Департамента лекарственных средств и медицинской техники и обновляется в реальном времени.
Особенность Кыргызстана в том, что страна не создавала свой стандарт QR-кодов. С помощью турецких специалистов система адаптирована для считывания кодов, разработанных для большинства стран, что облегчает импорт малых партий лекарств.
На сегодня в системе прослеживаемости лекарственных средств в Кыргызстане подключены 291 организаций здравоохранения и 2261 аптек.
АКИpress побеседовал со специалистами Департамента лекарственных средств и медицинских изделий о том, почему система важна для государства, какую пользу она принесет гражданам и как пациенты смогут проверять качество и подлинность лекарств.
В беседе приняли участие заместитель директора Департамента лекарственных средств и медицинских изделий Мариям Джанкорозова, заведующий отдела информационной и технической поддержки Департамента Нурадин Канатаев, разработчик мобильного приложения «Дары-Дармек» Мирбек Кудуретов.
— Система прослеживаемости лекарственных средств в Кыргызстане обсуждается уже давно. Ее внедрение началось при бывшем министре здравоохранения Таланта Батыралиеве, а в 2023 году с поддержкой государства и президента, стартовал второй этап реформы. Масштаб работы был действительно серьезным.
Мариям Джанкорозова: В настоящее время посредством цифровой маркировки могут прослеживаться различные потребительские товары, как например: сигареты, алкоголь, шубы или ювелирные изделия. Однако, важно понимать, что лекарства и медицинские изделия являются особым товаром, безопасность, эффективность и качество которого потребитель не может определить самостоятельно, в отличие от обычных товаров.
Поэтому, прослеживаемость лекарств и медицинских изделий является лишь частью широкой государственной регуляторной системы, которая имеет трехуровневый контроль безопасности, эффективности и качества фармацевтической продукции:
1) Государственная регистрация.
Лекарственные средства и медицинские изделия должны быть зарегистрированы в стране после проведения тщательной узкоспециализированной экспертизы. Для этого производитель подает регистрационное досье на продукцию в уполномоченный регуляторный орган (ДЛС и МИ при МЗ КР). В случае положительной экспертизы продукция производителя включается в государственный реестр зарегистрированных лекарств/медицинских изделий Кыргызстана или, при соответствующих процедурах, в реестр ЕАЭС. Только после регистрации разрешается использование препарата в медицинских целях и его ввоз в страну/производство в стране.
2) Пострегистрационный контроль за качеством продукции: при импорте/производстве в стране или отборе продукции непосредственно с рынка.
Каждая партия лекарства проходит оценку качества. Лабораторный контроль осуществляется на основе нормативных документов по качеству, которые содержат показатели качества и методики проверки. Только после успешной проверки конкретная серия лекарства допускается к обращению на рынке. Если производитель меняет технологию или состав препарата, в нормативный документ вносятся изменения. Следующие партии проверяются уже по обновленным методикам.
3) Фармаконадзор (ЛС)/мониторинг безопасности (МИ): наблюдение за безопасностью продукции уже находящейся на рынке страны путем сбора спонтанных сообщений либо путем активного фрамаконадзора.
В случае поступления сообщений о нежелательных реакциях на лекарство, особенно случаях жизнеугрожающих/опасных реакций использование лекарства должно быть приостановлено и проведено расследование, по результатам которого продукция может быть отозвана с рынка. В серьезных случаях у регулятора должна быть возможность оперативно приостановить использование конкретной серии лекарства, которое может одновременно находиться во всех звеньях цепочки поставок. Надо отметить, что для вышеуказанных случаев в ЭБД реализован функционал по приостановке использования препарата или его отзыва нажатием одной кнопки.
Все регуляторные меры также предполагают обязательное лицензирование субъектов фармацевтической деятельности, соблюдение правил надлежащей производственной практики (GMP), надлежащей дистрибьюторской практики (GDP) и т.д.
Система прослеживаемости интегрирована в этот многоэтапный регуляторный процесс: начиная с процедур государственной регистрации, контроля импорта и оценки качества каждой серии, далее через оптовые и розничные звенья, каждая упаковка лекарства контролируется на всех этапах движения. Это позволяет убедиться, что в страну поступает именно зарегистрированный препарат, а не подделка или фальсификат.
Таким образом, цифровизация системы лекарств охватывает весь регуляторный процесс: регистрация, импорт, оценка качества и собственно, прослеживаемость.
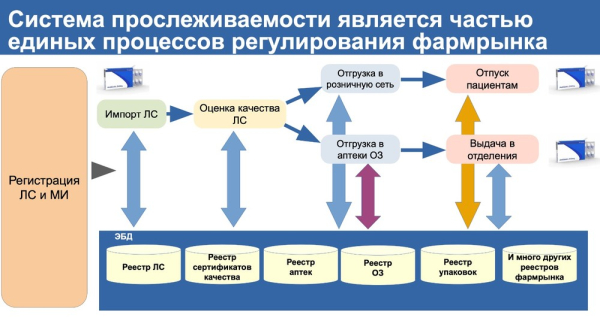
Автоматизация и информатизация нашей системы (ЭБД) полностью соответствует национальному законодательству в сфере обращения ЛС и МИ, благодаря чему обеспечена валидированная точка входа товара, то есть подтвержденный источник происхождения. Мы точно знаем, что препарат поступил именно с той производственной площадки, которая зарегистрирована и одобрена в процессе государственной регистрации продукции. Это принципиальное отличие от системы маркировки остальных товаров. В нашей системе нельзя просто приобрести QR-коды, наклеить их на продукцию и запустить ее в оборот, как это возможно в фискальных системах для других категорий товаров.
В случае с лекарствами система построена иначе: она начинается с регистрации производителя и препарата, а уже затем включается механизм прослеживаемости.
— Как лекарства попадают на рынок Кыргызстана?
Нурадин Канатаев: Для того, чтобы ввезти лекарство в страну и продавать в аптеках, должны быть соблюдены два условия: 1) препарат должен быть зарегистрирован в Кыргызстане и включён в государственный реестр, который генерируется из ЭБД (он является открытым на сайте Департамента); 2) каждая серия/партия должна пройти оценку качества в Департаменте.
Если отобранные образцы при оценке качества проходят лабораторный контроль и получают положительное заключение о качестве, серия/партия допускается к обращению в стране, а перечень всех выданных заключений через ЭБД публикуется на сайте департамента.
Кыргызстан — небольшая страна с относительно малым объемом потребления лекарств. Общий объём рынка лекарственных средств и медицинских изделий составляет около 30 млрд сомов, что сопоставимо с бюджетом одного малого европейского завода. Поэтому мы не можем диктовать мировым производителям дополнительные условия.
Если завод уже наносит маркировочный код — это удобно, и наша система способна считывать практически все международные форматы кодов. Если же производитель не печатает отдельные коды для Кыргызстана, мы не требуем этого, поскольку и без того предъявляем ряд сложно выполнимых для производителя требований, например, наличие инструкции на кыргызском языке.
Чтобы не усложнять процесс импорта, предусмотрена возможность нанесения стикеров с кодами внутри страны. При этом принцип остаётся неизменным: сколько упаковок ввезено в Кыргызстан, столько же кодов выдаётся и загружается в систему. Это и есть точка валидации, которая обеспечивает контроль объёма и подлинности продукции.
Мариям Джанкорозова: Да, этот момент важно отметить. Например, фискальные системы работают по другому принципу: оператор продаёт свои коды, сам их учитывает и затем отслеживает оборот по выданным кодам.
Наша система устроена иначе. Чтобы не создавать дефицит и не осложнять импорт из-за дополнительных требований, мы предусмотрели максимально гибкий механизм. Система способна считывать практически все международные форматы кодов.
Если у производителя нет подходящих кодов, наша система может генерировать их самостоятельно — при этом бесплатно. Это сделано для того, чтобы наши требования не стали причиной сокращения поставок, и чтобы население не столкнулось с нехваткой лекарств.
Таким образом, в систему загружаются коды только на те партии, которые прошли оценку качества. После этого начинается полноценная прослеживаемость каждой серии и каждой упаковки препарата.
— Про систему прослеживаемости: какое количество наименование лекарств прослеживается?
Нурадин Канатаев: В целом в стране зарегистрировано около 7000 наименований лекарств. Однако не все они фактически завозятся, и пока не все подпадают под прослеживаемость.
Мы не прослеживаем препараты стоимостью ниже 100 сомов, чтобы не влиять на их цену. Кроме того, существуют технические ограничения. Например, некоторые недорогие препараты выпускаются в бумажной упаковке с шероховатой поверхностью — сканер может не считать код, а стикер может просто отклеиться.
На сегодняшний день прослеживаемость охватывает около 2000 наименований.
Мариям Джанкорозова: важно понимать, что слово «прослеживаемость» — это конечный результат. До него есть большой этап автоматизации и цифровизации всей регуляторной системы.
Наша система — это не просто отслеживание товара, как в фискальных системах. Это бесшовная, линейная регуляторная система, которая начинается с регистрации препарата, затем включает процедуры импорта, оценки качества и только после этого прослеживаемость.
Все эти этапы закреплены законодательством: правила регистрации, ввоза и оценки качества определены постановлениями правительства. Кроме того, в наших отраслевых законах прямо указано, что система обращения лекарственных средств, медицинских изделий должна быть переведена в электронный формат управления.
Поэтому корректнее называть нашу систему электронной базой данных лекарственных средств и медицинских изделий, где прослеживаемость лишь один из модулей.
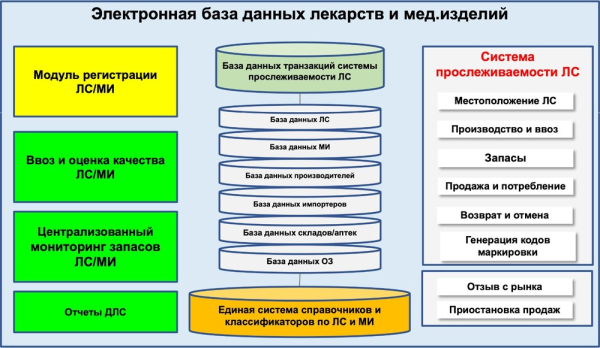
Фискальные системы для обычных товаров работают иначе. Для сигарет или других категорий не требуется государственная регистрация, где необходимо предоставить досье производителя, а лабораторная проверка проводится для каждой серии. Для лекарств же это обязательные этапы, поскольку речь идет о безопасности здоровья граждан.
Именно поэтому для лекарственных средств применяется более сложная и комплексная система, соответствующая требованиям законодательства.
— Если объяснить простыми словами для обычного гражданина: что изменилось после внедрения электронной базы данных? Люди ведь не видят внутренние процессы.
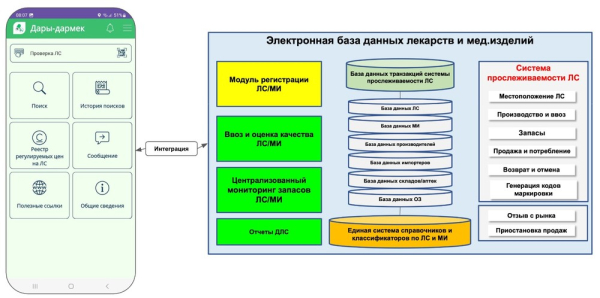
Мариям Джанкорозова: Главный результат для граждан, который они могут использовать — это мобильное приложение «Дары-Дармек». Все, что законно зарегистрировано и допущено к обращению на рынке, отражается в этом приложении.
Мирбек Кудуретов: Приложение интегрировано в ЭБД. В нем можно найти препарат и проверить, завезен ли он официально. Достаточно отсканировать QR-код на упаковке, и система покажет информацию о том, что лекарство прошло государственную регистрацию и оценку качества, а также отобразит номер сертификата качества.
Если при сканировании система сообщает, что такого препарата нет в базе, это означает, что он не был официально ввезен или не прошел лабораторную проверку (или пока не подлежит прослеживаемости для препаратов ниже 100 сом). Таким образом, покупатель может сразу убедиться в подлинности лекарства и обезопасить себя.
Кроме того, в приложении отображаются предельные розничные цены на препараты, стоимость которых регулируется государством. Если аптека продает лекарство дороже установленной цены, пользователь может подать жалобу прямо через приложение: выбрать препарат, прикрепить чек и указать свои контактные данные. Эти данные необходимы для того, чтобы уполномоченные органы могли официально зарегистрировать обращение.
Жалоба поступает в ЭБД, рассматривается, и заявитель получает обратную связь о результатах проверки.
Также в приложении можно открыть инструкцию к лекарству, ее можно просмотреть или скачать.
Таким образом, приложение позволяет гражданам проверять подлинность и качество препаратов, контролировать цены и при необходимости защищать свои права.
— Можно ли проверить наличие лекарств в стране?
Мирбек Кудуретов: да, можно. В приложении есть функция поиска: нужно ввести название препарата, и система покажет его наличие на карте Кыргызстана.
Чтобы не перегружать систему, для пользователя поиск отображает информацию в определенном радиусе, например, в пределах нескольких километров от местоположения пользователя.
— Можно ли сказать, что все аптеки страны подключены к системе прослеживаемости лекарственных средств?
Нурадин Канатаев: Фактически — да. Крупные дистрибьюторы, у которых аптеки закупают препараты, не отпускают товар тем, кто не зарегистрирован в системе. Передача лекарств возможна только через электронную базу данных, поэтому аптеки вынуждены подключаться.
Как Департамент лекарственных средств и медицинских изделий, мы видим полную картину по каждому препарату. Например, по конкретному лекарству система показывает, в каких медицинских организациях и аптеках оно есть и в каком количестве. Если одна упаковка списывается, остаток меняется в режиме онлайн. Мы можем увидеть данные по любому региону и по любой организации.
Мариям Джанкорозова: особенно важна эта система для препаратов, которые выдаются льготным категориям пациентов — людям с хроническими заболеваниями, эпилепсией, бронхиальной астмой и другими диагнозами. В будущем систему можно использовать для мониторинга ситуации о наличии лекарств. Если сопоставлять эти данные с реестром пациентов, можно более точно прогнозировать потребности. Например, контролировать наличие препаратов для паллиативной помощи или жизненно важных лекарств.
Система содержит данные об импорте и остатках, что позволяет анализировать ситуацию и предупреждать возможный дефицит. Кроме того, предусмотрен модуль Мониторинга запасов для государственных больниц: модуль позволяет видеть поступление лекарств в больницы и их движение там, независимо от того, прослеживается лекарство или нет, а также позволит перераспределять излишки между больницами. Этот модуль сейчас вводится в эксплуатацию. Это хороший инструмент для Министерства здравоохранения, которое будет иметь возможность видеть всю ситуацию по стране. Такой функционал очень важен для управления запасами особенно при различных чрезвычайных ситуациях.
Потенциал системы очень большой. При полном внедрении и развитии аналитических инструментов у Минздрава появятся большие возможности для улучшения лекарственного обеспечения населения.
— Сейчас работают два модуля. Еще три остались. Какие это модули?
Нурадин Канатаев: Это модули по регистрации лекарственных средств и медицинских изделий, их документооборот и интеграции с общими процессами ЕАЭС. Вот эти три модуля ещё не приняты, частично модуль регистрации по национальным правилам уже работают в боевом режиме, часть функционалов тестируется.
Мариям Джанкорозова: Изначально был принят модуль прослеживаемости, а также мониторинг запасов в больницах всего два модуля. Однако внедрили только один — прослеживаемость. Модуль мониторинга запасов в больницах только внедряется, так как не хватало людей до последнего времени. А модуль мониторинга запасов очень важен для эффективного управления запасами, особенно для Минздрава.
Например, чтобы отслеживать наличие лекарств в лечебной сети, те же инсулины, например. Инсулины поставляет государство и распределяет по всей лечебной сети. Потом оказывается, что в одном месте препарат в избытке, а в другом месте его не хватает. Это ведь не коммерческая поставка, поэтому Минздрав мог бы оперативно перераспределять препараты по стране.
Сейчас Минздрав формирует реестр диабетиков. Если все это связать в единую систему, можно будет учитывать потребности каждого пациента, так как инсулин бывает разных видов и каждому пациенту нужен определенный. Тогда распределение станет более адресным и точным.
ЭБД сопровождает весь законодательный цикл обращения лекарственных средств — весь необходимый функционал предусмотрен. Например, есть функции, связанные со сроками годности: видно, когда срок истекает.
Если по каким-то причинам, связанным с жизнеугрожающей ситуацией, нужно срочно отозвать препарат с рынка все аптеки будут оповещены об этом в системе – будет стоять запрет на продажу конкретной серии препарата.
— Более 25 млн упаковок выведены из обращения. Видно ли, сколько лекарств уже использовано?
Нурадин Канатаев: У нас вывод отображается сразу. Мы можем видеть, кто сколько использовал и сколько вывел из обращения. Это помогает прослеживать движение препарата до конечного потребителя.
Полная информация о том, какой пациент получил лекарство, станет доступна после интеграции с электронной системой рецептов. Этот процесс ведет Минздрав, поэтому пока данных до конечного пациента у нас нет.
— Система прослеживаемости снижает коррупционные риски на рынке лекарств?
Мариям Джанкорозова: Да, и здесь важно понять механизм. Если речь идет о нормативных документах по качеству, то лабораторный контроль не всегда обязателен для надежных производителей и прямых поставок. Для таких поставок достаточно документального контроля — подтверждения того, что препарат произведен и поставлен именно от проверенного производителя. Это сокращает избыточные регуляторные процедуры, экономит время и снижает затраты, не замедляя доступ препаратов к пациентам.
Цифровизация регуляторной системы делает работу регулятора и субъектов фармрынка прозрачной. Все решения и процедуры регулятора фиксируются в ЭБД, их невозможно будет подменить вручную после полного ввода всех модулей. Это должно снизить все коррупционные составляющие в фармацевтическом секторе страны.
Таким образом, ЭБД задумана как мощный антикоррупционный инструмент: она повышает подотчётность регулятора, предотвращает попадание фальсифицированных и контрабандных препаратов на рынок, защищая население, а также укрепляет доверие граждан к государству и системе здравоохранения.
— С помощью системы удалось ли хоть как-то контролировать и снизить контрабанду? Есть ли какие-то результаты?
Нурадин Канатаев: Да, результаты есть. Например, многие медицинские центры начали закупать лекарства только у официальных дистрибьюторов. Раньше это делали единицы, сейчас все центры переходят с «черного рынка» на официальные поставки.
Кроме того, по данным ассоциации фармпроизводителей и поставщиков за 2022 год, доля контрабандных лекарств составляла около 30-40 процентов. С каждым годом объем официально ввезённых лекарств растет примерно на 2 млрд сомов, при этом потребление практически не меняется. Это показывает, что доля контрабанды снижается, а пропорция официально завезённых препаратов увеличивается.
Мариям Джанкорозова: Кроме того, ЭБД дает возможность со временем отслеживать утечку препаратов из официального оборота в нелегальный (базар). Если, например, лекарство из больницы попало в частную аптеку или базар, его можно будет определить по уникальному QR-коду и узнать откуда была утечка . Пока этим не все активно пользуются, но такая возможность уже есть, и это дополнительно повышает контроль и снижает риски неофициального оборота.
— На заседании коллегии Минздрава руководство говорило о том, что завершить полностью работу системы прослеживаемости лекарственных средств. Уже ведется ведь работа?
Нурадин Канатаев: Есть приказ о том, чтобы мы приняли модуль регистрации лекарственных средств. Сейчас работает комиссия по приёмке, уже прошло два заседания, сегодня комиссия собирается третий раз, то есть процесс идёт. Опять же надо отметить, что речь идет об ЭБД, когда говорят о прослеживаемости.
— Можно ли сказать, что система полностью заработает в течение года?
Мариям Джанкорозова: сама система прослеживаемости работает полностью. Модуль прослеживаемости была принят ещё в 2022 году: её запустили по всей стране, провели обучение и сейчас она функционирует.
То, что еще не завершено, — это модули по регистрации лекарств и медицинских изделий. Люди иногда путают: думают, что система «не работает», но на самом деле прослеживаемость функционирует. Осталось доработать именно регистрационную часть, документооборот и интеграцию с Общими процессами ЕАЭС.
Регистрация — это сложный экспертный процесс: изучение досье на тысячи страниц, фармакологическая, фармацевтическая экспертизы и лабораторные испытания. Обычная регистрация занимает около 180 дней, есть и ускоренные процедуры для строгих регуляторов и производителей, преквалифицированных ВОЗ . Сейчас этот процесс полностью оцифровывается: подача заявок онлайн, распределение по экспертам, отслеживание времени экспертных работ, очередности заявок, фиксирование результатов экспертизы и решений в цифровом формате, выдача электронного регистрационного удостоверения, выход данных в государственный реестр.
Часть регистрации уже работает в «боевом» режиме, включая формирование счетов и взаимодействие с лабораториями. Оставшиеся этапы — приемка регистрации по медицинским изделиям, что завершит оцифровку национальных процедур регистрации.
— Можете ли рассказать, как работает импорт и проверка документов на лекарства?
Нурадин Канатаев: Каждая заявка включает все необходимые документы — контракт, инвойс, сертификаты качества, товаросопроводительные документы и др.
Для одного продукта мы видим полный набор документов. Поставщик загружает их в систему через личный кабинет. После проверки нашими сотрудниками заявки направляются в таможню, где формируется электронная таможенная папка. Все происходит онлайн — таможенные брокеры и ГТС сразу получают доступ к документам.
Мариям Джанкорозова: Справки для таможенной очистки подписываются обычно в течение одного дня. Около 80-90% выдаются день в день. После этого проводится таможенная очистка, а затем следующим этапом по системе продукция переходит на процедуру оценки качества.
— Что происходит при выявлении ошибок в документах?
Нурадин Канатаев: Если есть несоответствия, например, отсутствует штрих-код — заявка возвращается на доработку. После исправления она снова проходит проверку.
Все заключения о качестве доступны в реестре Департамента лекарственных средств на сайте. Любая больница или гражданин может проверить конкретную партию товара на сайте, убедиться, что она официально завезена и прошла лабораторный контроль.
— Что получит государство, когда система заработает в полном объёме?
Мариям Джанкорозова: В целом, государство получит полную прозрачность работы регулятора и его подотчетность в принятии решений по всем его регуляторным процедурам, также всего фармацевтического рынка.
Прозрачность рынка — это показатель надлежащего государственного регулирования. Также это позволит
Оперативно получать информацию о движении ЛС и МИ по всей цепи поставок, запасах, потреблении и др. аналитическую информацию
Оперативно и адекватно принимать управленческие решения на основе достоверных данных.
Это повысит информированность и безопасность граждан, которые используют лекарства и медицинские изделия.
Система повысит эффективность работы регулятора, скорость процедур за счет уменьшения ручных процессов. Раньше регистрационные досье на ЛС и МИ хранились в архивах, что затрудняло работу с ними. В будущем все досье будут в электронном виде в ЭБД. Если требуется расследование по качеству, можно быстро проверить всю документацию, провести отбор образцов и повторное испытание. Вся цепочка поставок уже оцифрована, что ускоряет процессы и снижает ошибки и другие коррупционные риски системы.

 НОВОСТИ В КЫРГЫЗСТАНЕ
НОВОСТИ В КЫРГЫЗСТАНЕ